Асоціація дитячих офтальмологів та оптометристів України
Існуємо з 2001 року.
Ми є неприбутковою громадською організацією, яка об’єднує громадян,
котрі виявили бажання співпрацювати для реалізації Статутних завдань Асоціації.
Мета
Є сприяння науковому і практичному розв’язанню сучасних проблем медичного обслуговування населення, підвищення рівня кваліфікації та захист соціальних, економічних, творчих, культурних та інших спільних інтересів членів Асоціації.
Завдання та основні напрями діяльності
- сприяння розробці пріоритетних напрямів розвитку медичного обслуговування дітей, їх батьків та іншого дорослого населення, які страждають на захворювання очей та визначенню загальної політики з цих питань;
- вивчення сучасних досягнень в галузі офтальмології;
- організація та проведення різноманітних у тому числі міжнародних науково-практичних конференцій, форумів, семінарів , симпозіумів, виставок, тренінгів, інтерактивних заходів з виданням сертифікатів, дипломів та свідоцтва щодо участі у таких заходах;
- здійснення інформаційно-роз’яснювальної діяльності для дітей та дорослого населення (у тому числі в дитячих дошкільних закладах, закладах освіти, вищих навчальних закладах), а також для лікарів, освітян та фахівців інших спеціальностей.
Загальна кількість членів Асоціації (станом на 13 лютого 2018 року) – 389 осіб.
Голова правління - Риков Сергій Олександрович, тел. (050) 534-60-09
Заступник Голови Правління – Сенякіна Антуанета Степанівна, тел. (050) 548-85-83
Виконавчий директор – Алеєва Наталія Миколаївна, тел. (067) 707-09-93
Фінансовий директор – Чувалова Жанна Володимирівна, тел. (067) 967-47-07
Новини асоціації

Новини
Як соцмережі виснажують наш зір: нове дослідження про вплив смартфонів на очі

Очні краплі проти пресбіопії: нове дослідження підтверджує їхню ефективність і безпеку на період до двох років
З віком в усіх людей розвивається пресбіопія — утруднене фокусування на близьких об’єктах і тексті, через що часто доводиться користуватися окулярами для читання. Проте вирішення проблеми може бути таким простим, як застосування спеціальних очних крапель два-три рази на день.
Ретроспективне дослідження 766 пацієнтів, представлене на 43-му Конгресі Європейського товариства катарактальних і рефракційних хірургів (ESCRS), показало: більшість учасників змогли прочитати на дві, три або більше ліній більше на таблиці Єгера (шкалі для перевірки гостроти зору поблизу) після використання спеціально розроблених крапель. Ефект зберігався до двох років.
Д-р Джованна Беноцці, директорка Центру передових досліджень пресбіопії в Буенос-Айресі (Аргентина), пояснила:
«Ми провели це дослідження, адже існує значний незадоволений попит на ефективне лікування пресбіопії. Поточні методи — окуляри для читання чи хірургічні втручання — мають свої недоліки: незручність, соціальний дискомфорт, а також потенційні ризики й ускладнення.
Є група пацієнтів із пресбіопією, які не можуть або не хочуть користуватися окулярами й водночас не є кандидатами на операцію. Саме для них ми шукали доказову неінвазивну, зручну та дієву альтернативу».
Очні краплі, створені покійним доктором Хорхе Беноцці, батьком дослідниці, поєднують дві діючі речовини: пілокарпін (звужує зіницю та активує війковий м’яз, що регулює акомодацію ока) і диклофенак — нестероїдний протизапальний засіб, який зменшує запалення та дискомфорт, що іноді спричиняє пілокарпін.
Пацієнти закапували краплі двічі на день — зазвичай після пробудження та через шість годин. За потреби дозволялася третя доза для додаткового комфорту. Учасників (373 жінки й 393 чоловіки, середній вік — 55 років) поділили на три групи, кожна з яких отримувала препарат із однаковою дозою диклофенаку, але з різною концентрацією пілокарпіну: 1 %, 2 % або 3 %.
Дослідники оцінили, наскільки добре пацієнти могли читати таблицю Єгера без окулярів (нескоригована гострота зору поблизу) через годину після першого закапування й продовжили спостереження протягом двох років.
Д-р Беноцці повідомила:
«Найважливіший результат нашої роботи — швидке та тривале покращення зору поблизу для всіх трьох концентрацій. Уже через годину після першої дози середній показник покращився на 3,45 лінії за шкалою Єгера. Краплі також сприяли кращому фокусуванню на різних відстанях.
99 % пацієнтів у групі з 1 % пілокарпіну змогли прочитати щонайменше дві додаткові лінії, а близько 83 % усіх учасників зберегли добрий зір поблизу через рік. Важливо, що ми не спостерігали серйозних побічних ефектів, таких як підвищений внутрішньоочний тиск чи відшарування сітківки».
У групі з 2 % пілокарпіну 69 % пацієнтів змогли прочитати щонайменше три додаткові лінії, а в групі з 3 % — 84 %. Покращення трималося до двох років (у середньому 434 дні). Побічні явища були незначними: тимчасове затуманення зору (32 %), подразнення при закапуванні (3,7 %) та головний біль (3,8 %). Жоден учасник не припинив лікування.
Серед відомих побічних ефектів пілокарпіну: почервоніння очей, сльозотеча, розмитість зору, підвищена чутливість до світла, труднощі з фокусуванням між різними об’єктами, спалахи світла чи «мушок» у полі зору, а в рідкісних випадках — відшарування сітківки.
Дослідниця додала:
«Майже всі пацієнти відзначили позитивний ефект, але його ступінь залежав від початкової гостроти зору. Наші дані свідчать: оптимальну концентрацію пілокарпіну слід добирати індивідуально, зважаючи на тяжкість пресбіопії. Пацієнти з легкою формою найкраще реагували на 1 % розчин, а з вираженішими проявами потребували 2 % або 3 %».
Вона підсумувала:
«Ця комбінована терапія є безпечною, ефективною та добре переноситься. Вона може істотно зменшити залежність від окулярів для читання, пропонуючи зручний і неінвазивний варіант, хоча не всім людям краплі повністю замінять окуляри.
Лікування не призначене для заміни хірургії, але є цінною опцією для тих, хто прагне уникнути дискомфорту, пов’язаного з окулярами. Тепер офтальмологи мають доказову фармакологічну альтернативу, яка розширює можливості лікування пресбіопії».
Крім учасників дослідження, у д-ра Беноцці є пацієнти, що користуються цими краплями вже понад десять років. Вона планує додаткові дослідження, щоб оцінити вплив препарату на якість життя та краще зрозуміти його механізм дії.
Сильними сторонами роботи є велика вибірка та тривалий період спостереження. Це перше систематичне дослідження, яке порівнює три концентрації пілокарпіну в комбінації з диклофенаком. Серед обмежень — ретроспективний, одноцентровий характер, що може вплинути на узагальнення результатів і призвести до упередженості вибірки.
Обраний президент ESCRS, професор Буркхард Дік, завідувач офтальмологічного відділення Університетської очної клініки Бохума (Німеччина), який не брав участі в дослідженні, зазначив:
«Хоча хірургічні методи корекції вікових змін зору розвиваються, деякі пацієнти не можуть їх використовувати. Робота д-ра Беноцці показує, що краплі з пілокарпіном і диклофенаком здатні покращити зір поблизу на строк до двох років, але через обмеження дизайну дослідження ці результати не можна автоматично поширювати на всіх.
Тривале використання пілокарпіну може знижувати нічний зір, ускладнювати бачення в темряві, викликати втому очей чи подразнення, а тривале застосування НПЗЗ іноді шкодить рогівці. Необхідні масштабні багатопрофільні дослідження, щоб остаточно підтвердити безпеку й ефективність цього методу перед його широким впровадженням».
Оригінальна стаття була опублікован на порталі Medical Xpress 14 вересня 2025 року.
Лазерна корекція зору для старших підлітків: масштабне дослідження підтвердило безпеку та ефективність процедури
Згідно з дослідженням, представленим на 43-му Конгресі Європейського товариства катарактальних і рефракційних хірургів (ESCRS), масштабне вивчення лазерної корекції короткозорості свідчить, що ця процедура є такою ж безпечною та ефективною у старших підлітків, як і в дорослих.
Короткозорість, або міопія, вражає приблизно третину дітей та підлітків, і дослідження показують, що її поширеність постійно зростає.
Лазерне лікування, відоме як фоторефракційна кератектомія (ФРК), широко застосовується для корекції міопії в дорослих, однак досі існували питання щодо його використання у підлітків.
Нове дослідження представив доктор Авіноам Шай із відділення офтальмології медичного центру Rambam у Хайфі (Ізраїль).
Він пояснив:
«Деякі лікарі хвилюються, що очі підлітків можуть ще змінюватися або що їхня рогівка може по-іншому реагувати на загоєння після лазерного втручання, що підвищує ризик побічних ефектів. Однак у певних випадках підлітки прагнуть постійного вирішення своєї проблеми з міопією.
Ми помітили, що багато пацієнтів віком 17–18 років досягають чудових результатів, незважаючи на ці побоювання. Це й спонукало нас дослідити, чи справді ФРК є безпечним і ефективним для цієї вікової групи».
У дослідженні проаналізували дані пацієнтів із міопією, яких лікували методом ФРК у лазерних центрах Care-Vision у Тель-Авіві з січня 2010 до червня 2024 року. Загалом було проліковано 65 211 очей.
ФРК передбачає використання лазера для видалення тонкого шару тканини з рогівки — прозорого куполоподібного покриву, що захищає зіницю та райдужку. Рогівка виконує роль «вікна» для світла, тож зміна її форми допомагає поліпшити фокусування зображення на сітківці та скорегувати проблеми із зором, зокрема короткозорість.
Команда доктора Шая розділила пацієнтів за віком, щоб порівняти ефективність процедури у групі 17–18 років та у дорослих віком 19–40 років.
Результати показали, що у старших підлітків ефективність була такою ж високою, а подекуди навіть кращою, ніж у дорослих: близько 64 % очей підлітків досягли гостроти зору 20/20 (нормальний зір) порівняно з 59 % у дорослих.
Частка очей, яким знадобилася повторна процедура, в обох групах була дуже низькою — лише 0,41 %. Такі ускладнення, як затуманений зір або ослаблення рогівки (ектазія), також траплялися вкрай рідко.
Доктор Шай підсумував:
«Це, без сумніву, найбільше дослідження ФРК у підлітків, а такий великий обсяг вибірки робить результати дуже надійними. Водночас слід пам’ятати, що це ретроспективне дослідження, тобто ми аналізували вже наявні дані, а не проводили новий експеримент від початку.
Наші висновки свідчать: для ретельно обстежених підлітків зі стабільною короткозорістю ФРК може бути безпечним і ефективним рішенням, особливо якщо окуляри чи контактні лінзи не підходять. Сам лише вік не має бути перешкодою для мотивованого та добре підготовленого підлітка».
Дослідники планують і надалі спостерігати за підлітками, які пройшли лазерну корекцію, щоб виявити можливі віддалені ускладнення або зміни зору.
Професор Томас Конен, голова публікаційного комітету ESCRS та директор кафедри офтальмології Університету Гете у Франкфурті (Німеччина), який не брав участі в дослідженні, прокоментував:
«Поширеність короткозорості серед дітей і підлітків зростає в усьому світі, і вона може погіршуватися до 30 років. У дитячому віці міопію зазвичай коригують окулярами або контактними лінзами, тоді як дорослі мають можливість обрати лазерне лікування.
Це масштабне когортне дослідження фоторефракційної кератектомії для лікування короткозорості показало, що процедура є безпечною та ефективною для старших підлітків. Це свідчить, що для деяких молодих людей вона може стати альтернативою окулярам або контактним лінзам».
Оригінальна стаття була опублікована на порталі Medical Xpress 15 вересня 2025 року.
Дані дослідження були представлені на 43-му Конгресі Європейського товариства катарактальних і рефракційних хірургів (ESCRS).
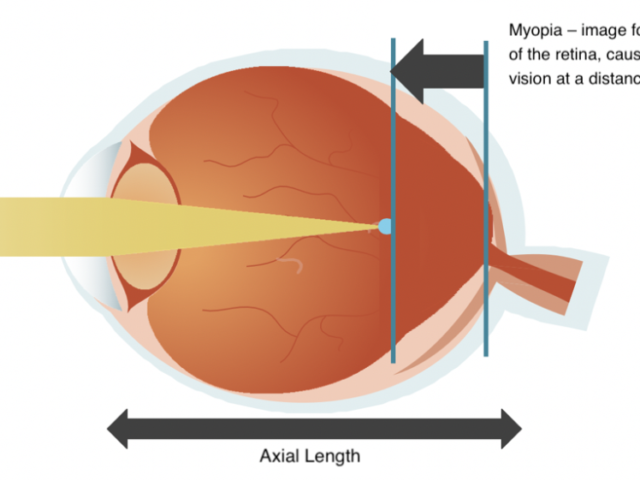
Вища відносна периферична рефракція пов’язана з прискореним розвитком міопії в дітей — дані МРТ-дослідження
Нові дані з дослідження, опублікованого 16 червня в American Journal of Ophthalmology, вказують, що як горизонтальна, так і вертикальна відносна периферична рефракція (ВПР) пов’язані зі швидшим прогресуванням осьової довжини ока та підвищеним ризиком розвитку короткозорості у дітей.
Дослідники на чолі з д-ром Сандером К.М. Кнепкенсом (Erasmus Medical Center, Роттердам, Нідерланди) використали інноваційний підхід — індивідуалізоване трасування променів на основі магнітно-резонансної томографії (МРТ), щоб вивчити просторові особливості рефракційних змін сітківки у дітей.
У дослідженні взяли участь 1635 дітей, яких обстежували офтальмологічно у віці 9 і 13 років. За даними МРТ, ВПР була більш гіперметропічною в дітей із короткозорістю, що узгоджувалося як для горизонтального, так і для вертикального напрямів. Вищий горизонтальний і вертикальний радіус кривизни сітківки (RPR) корелював з більшою осьовою довжиною ока, менш позитивним сферичним еквівалентом і вищим ризиком розвитку міопії.
Статистичний аналіз показав, що кожне збільшення ВПР на 1 D асоціювалося з вищим ризиком виникнення короткозорості: коефіцієнти шансів становили 1,40 (горизонтальна ВПР) та 1,29 (вертикальна ВПР).
«Ми виявили, що вища ВПР тісно пов’язана як зі швидшим зростанням осьової довжини, так і зі збільшенням ризику розвитку міопії», — зазначають автори. «Наші результати підтверджують важливість ВПР як предиктора прогресування короткозорості й можуть стати основою для розробки таргетованих методів контролю міопії в дітей».
Це дослідження є важливим кроком до глибшого розуміння біомеханіки очного яблука в дитячому віці та має потенціал для вдосконалення профілактичних та терапевтичних стратегій у сфері контролю міопії.
Оригінальне дослідження було опубліковане в журналі American Journal of Ophthalmology в 2025 році.

Як ранній візуальний досвід формує зорові шляхи мозку
Дослідники з Массачусетського технологічного інституту (MIT) виявили, що ранній візуальний досвід новонароджених може мати ключове значення для формування двох основних зорових шляхів у мозку. Один із них відповідає за обробку кольору та дрібних деталей (парвоцелюлярний шлях), інший — за просторову локалізацію та швидке виявлення руху (магноцелюлярний шлях).
Вплив обмеженого зору у новонароджених
Новонароджені мають нечіткий зір і слабке кольорове сприйняття через незрілість колбочок сітківки. Науковці припускають, що така візуальна «обмеженість» не є недоліком, а може допомагати мозку спеціалізувати клітини на обробці інформації з низькою просторовою і кольоровою частотою — тобто, сприяти розвитку магноцелюлярного шляху. Згодом, коли зір стає чіткішим і насиченішим, активізується розвиток парвоцелюлярного шляху.
Обчислювальні моделі розвитку зору
Щоб перевірити цю гіпотезу, дослідники створили комп’ютерні моделі, які на початку навчалися на розмитих сірих зображеннях, а потім — на чітких повнокольорових. Результат: моделі формували окремі «нейроноподібні» одиниці, що функціонально нагадували магно- та парвоцелюлярні шляхи. Моделі, які навчалися лише на якісних повнокольорових зображеннях, таких результатів не демонстрували.
«Результати потенційно вказують на механізм формування поділу на парво- та магноцелюлярні шляхи — один із ключових принципів організації зорової системи мозку», — зазначає професор Паван Сінха, керівник дослідження.
Дані з реального досвіду
Гіпотеза команди MIT ґрунтується не лише на теорії, а й на спостереженнях за дітьми з оборотною втратою зору — зокрема, після операцій з видалення вродженої катаракти. Дослідження показали, що після відновлення зору діти краще розпізнають об’єкти на кольорових зображеннях, ніж на чорно-білих, що вказує на важливість початкового обмеженого кольорового сприйняття для розвитку стійкого розпізнавання.
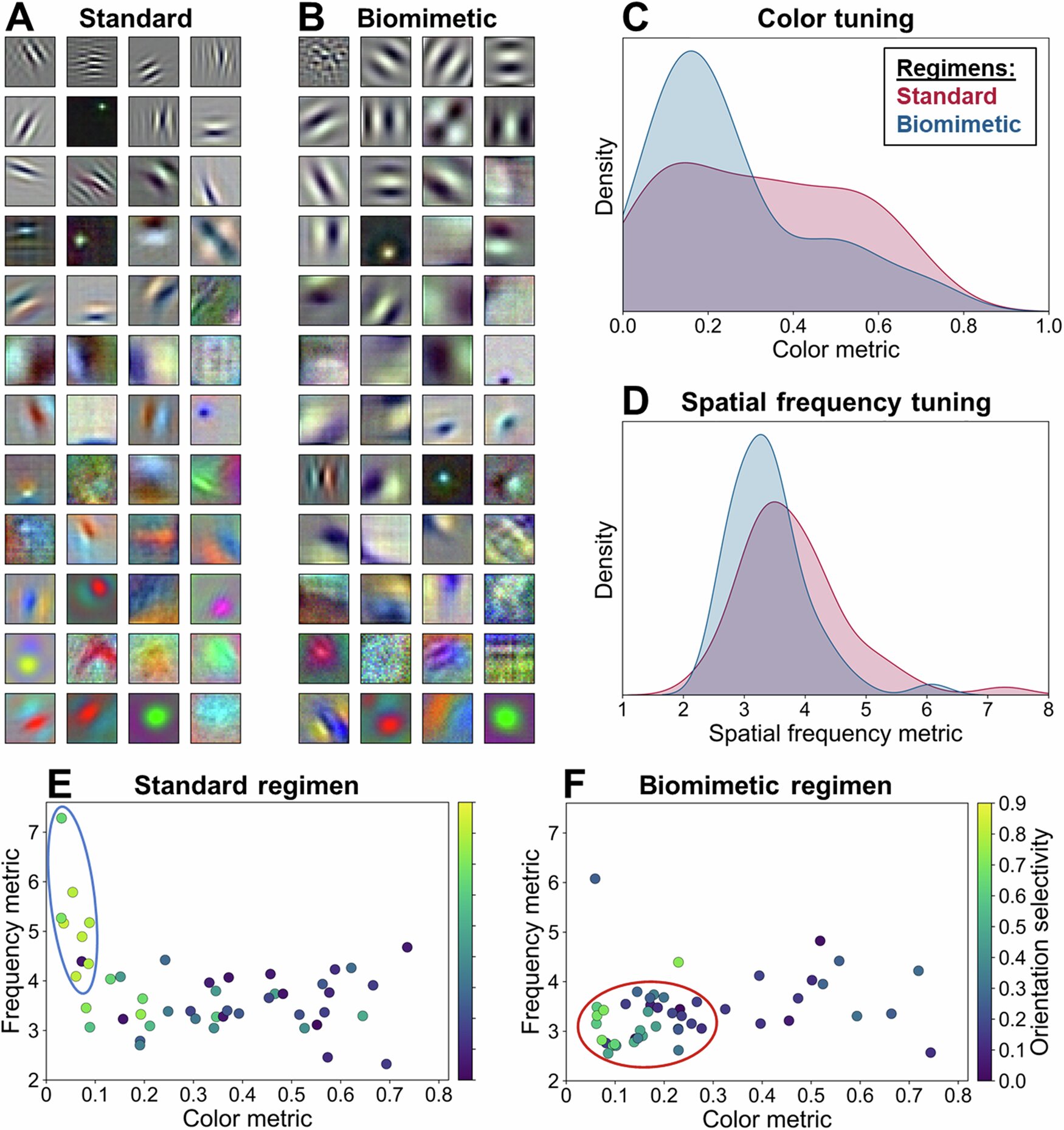
Структура моделей і аналіз
У ході аналізу дослідники помітили, що моделі, навчені на «біоміметичних» (наближених до реальних дитячих) зображеннях, розвинули дві окремі групи одиниць:
- Магноцелюлярноподібні — реагували на низькі просторові частоти та сірі тони.
- Парвоцелюлярноподібні — спеціалізувалися на вищих частотах і насичених кольорах.
Таке розмежування відсутнє у моделях, які з самого початку навчалися на високоякісних зображеннях.
Розпізнавання об’єктів і часовий вимір
Моделі, навчені за біоміметичним підходом, краще розпізнавали форму об’єктів (наприклад, кіт із текстурою слона), що узгоджується з людською стратегією категоризації. Видалення магноцелюлярноподібних одиниць зменшувало здатність моделей орієнтуватися на форму.
Також дослідники використовували відеодані для введення часового параметра. Моделі, натреновані на біоміметичних відео, демонстрували високу чутливість до швидких змін, що підтверджує роль магноцелюлярного шляху у сприйнятті руху.
Висновки
Отримані дані свідчать, що ранній обмежений зоровий досвід — у вигляді розмитих, чорно-білих зображень — може бути не лише адаптивним, а й критично важливим для правильної організації зорових шляхів. Ці результати не виключають ролі генетики, але вказують, що досвід має потужний вплив на формування зорової системи.
«Розвиток зору — це не просто дозрівання, а гнучкий процес, тісно пов’язаний з якістю сенсорного входу. Це відкриває перспективи для реабілітації та корекції порушень зору у дітей», — зазначає професор Сінха.
Оригінальна стаття була опублікована у журналі Communications Biology 3 липня 2025 року.
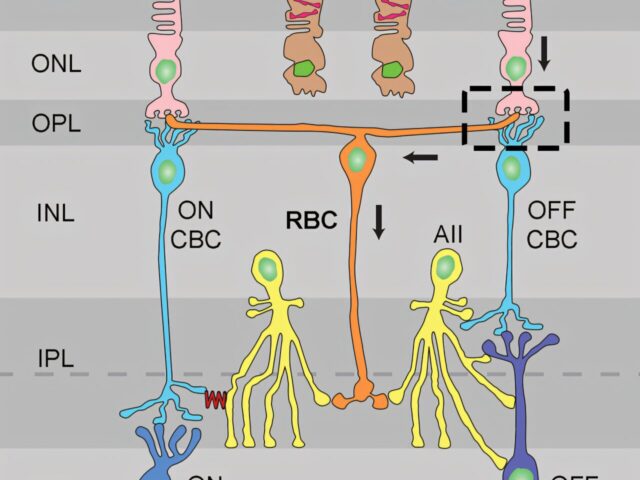
Сітківка здатна до переналаштування при пігментному ретиніті — нові перспективи для збереження зору
Дослідники з Інституту очних хвороб імені Джулса Штайна при Медичній школі Девіда Геффена (Каліфорнійський університет, Лос-Анджелес) виявили, що певні клітини сітківки можуть адаптуватися до втрати зору, пов’язаної з пігментним ретинітом — спадковим захворюванням, що поступово призводить до сліпоти.
У дослідженні, проведеному на мишачих моделях, науковці встановили, що паличкоподібні біполярні клітини — нейрони, які зазвичай отримують сигнали від паличок (фоторецепторів, відповідальних за нічний зір), — здатні формувати нові функціональні зв’язки з колбочками, що відповідають за денний і кольоровий зір. Це відбувається тоді, коли палички втрачають здатність до функціонування. Результати опубліковані в журналі Current Biology.
Пігментний ретиніт уражає мільйони людей у світі та є однією з провідних причин спадкової втрати зору. Незважаючи на те, що хвороба прогресує повільно, а деякі пацієнти зберігають зір до середнього віку, механізми адаптації сітківки до втрати клітин залишаються погано вивченими. Вивчення таких механізмів може відкрити нові терапевтичні цілі для збереження зору.
У своїй роботі дослідники використали мишей з нокаутом гена родопсину — моделі ранньої форми пігментного ретиніту, при якій палички не здатні реагувати на світло, однак дегенерація відбувається поступово. Вони проводили електрофізіологічні записи з окремих паличкоподібних біполярних клітин, щоб з’ясувати, як ці нейрони реагують на втрату свого типового джерела сигналу.
Також були використані додаткові моделі мишей з різними порушеннями паличкового каскаду сигналізації, що дозволило визначити фактори, які запускають процес переналаштування. Отримані дані підтверджувалися електричними вимірюваннями активності всієї сітківки.
У мишей, які втратили функціональні палички, паличкоподібні біполярні клітини виявили неочікувану активність — сильні реакції, спричинені сигналами від колбочок. Ці нові зв’язки мали характерну електрофізіологічну відповідь, типову для колбочок, а не паличок.
Важливо, що таке переналаштування відбувалося лише в умовах справжньої дегенерації паличок, а не просто за відсутності їх реакції на світло. Це вказує на те, що тригером змін є саме процес дегенерації, а не функціональна бездіяльність або пошкодження синапсів.
Отримані результати доповнюють попередні дослідження цієї ж групи 2023 року, які довели, що колбочки можуть залишатися функціональними навіть після суттєвих структурних змін на пізніх стадіях захворювання. Сукупно ці роботи демонструють здатність сітківки до адаптації та підтримки зорової функції завдяки різним механізмам на різних етапах прогресування патології.
За словами провідного автора дослідження, доктора філософії А. П. Сампата, «сітківка має здатність адаптуватися до втрати паличок, зберігаючи денну світлочутливість. Коли традиційні зв’язки між паличками й біполярними клітинами руйнуються, останні можуть переключитися на взаємодію з колбочками».
Механізм цієї пластичності, ймовірно, пов’язаний із процесами, що супроводжують дегенерацію, зокрема дією гліальних клітин чи сигналами, які вивільняються під час загибелі нейронів.
Наразі команда продовжує дослідження на інших генетичних моделях, включаючи мишей із мутаціями в генах родопсину та інших білків паличок, що також асоціюються з пігментним ретинітом у людей. Вчені прагнуть з’ясувати, чи є виявлений механізм переналаштування універсальним для цього типу дегенеративних змін.
Оригінальне дослідження було опубліковане в журналі Current Biology 7 лпиня 2025 року.
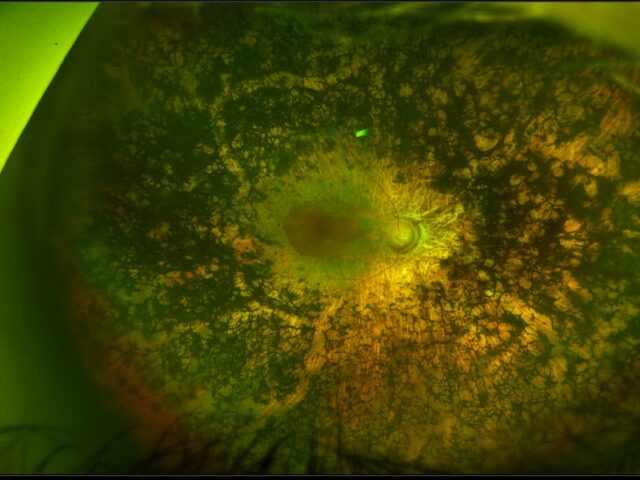
Нові кроки у розробці генетичної терапії для пізніх стадій спадкових дегенерацій сітківки
Спадкові дегенерації сітківки (СДС, англ. IRD — inherited retinal degenerations) — це група генетичних захворювань, які зумовлюють прогресивну втрату зору внаслідок загибелі фоторецепторів — світлочутливих клітин сітківки. Причиною цього є мутації в генах, критично важливих для функціонування та виживання фоторецепторів.
Генна терапія вже давно розглядається як перспективна стратегія для відновлення або збереження зору. Проте більшість існуючих методів орієнтовані на ранні стадії захворювання, коли ще не настала значна загибель фоторецепторів. Це створює серйозну прогалину в терапевтичних можливостях для пацієнтів, яким діагноз встановлюється на пізніших етапах.
Прорив у Penn Vet: потужні промотори для дегенерованої сітківки
Дослідники з Відділу експериментальної терапії сітківки Школи ветеринарної медицини Університету Пенсильванії (Penn Vet) у співпраці з іншими установами повідомили про створення нового набору високоспецифічних промоторів для фоторецепторів. Результати опубліковані в журналі Molecular Therapy.
Команду очолювали:
- д-р Рагхаві Судхарсан, доцент експериментальної офтальмології Penn Vet
- проф. Вільям А. Белтран, керівник відділу, професор офтальмології імені Корінн Р. Генрі Бауер
Вчені розробили чотири нові короткі ДНК-послідовності (промотори), які ефективно активують терапевтичні гени в паличках і колбочках навіть тоді, коли понад половина фоторецепторів уже втрачена.
«Ці промотори працюють як молекулярні перемикачі, які активують цільові гени безпосередньо в клітинах, що збереглися, забезпечуючи високу експресію навіть на пізніх стадіях захворювання», — пояснює Судхарсан.
Вищі за ефективністю, менші за розміром
У порівнянні зі стандартним промотором GRK1, нові конструкції продемонстрували вищу силу та специфічність експресії, зокрема промотори на основі гену GNGT2. Вони були активними як у паличках, так і в колбочках, і мають розмір менше 850 пар основ, що робить їх ідеальними для доставки за допомогою аденоасоційованого вірусу (AAV).
Більшість традиційних промоторів для колбочок є значно більшими і можуть не поміститися в межах обмеженого обсягу AAV-векторів.
«Малий розмір і клітинна специфічність знижують ризик побічних ефектів і зменшують потенційні імунні реакції — ключові фактори при розробці безпечної довготривалої терапії», — зазначив Белтран.
Як це вдалося?
Команда використала поєднання in silico моделювання, транскриптомного аналізу та in vivo тестування на великих тваринних моделях, які імітують людські форми IRD. Відповідно, тестування проводилося не в клітинних культурах чи органоїдах, а в повноцінних клінічно релевантних умовах.
Серед найбільш перспективних промоторів — ті, що отримані з генів GNGT2, IMPG2 та PDE6H, які демонстрували стабільну та високо специфічну експресію після доставки через AAV у сітківки собак з дегенеративними захворюваннями сітківки.
«Це дослідження відкриває новий шлях до генної терапії для пацієнтів на пізніх стадіях IRD — саме там, де наразі відчувається найбільший дефіцит ефективних методів лікування», — підсумовує Судхарсан.
Оригінальне дослідження було опубліковане в журналі Molecular Therapy 21 травня 2025 року.
Наша команда

Риков Сергій Олександрович
Голова правління

Сенякіна Антуанетта Степанівна
Заступник Голови Правління

Чувалова Жанна Володимирівна
Фінансовий директор

Алеєва Наталія Миколаївна

