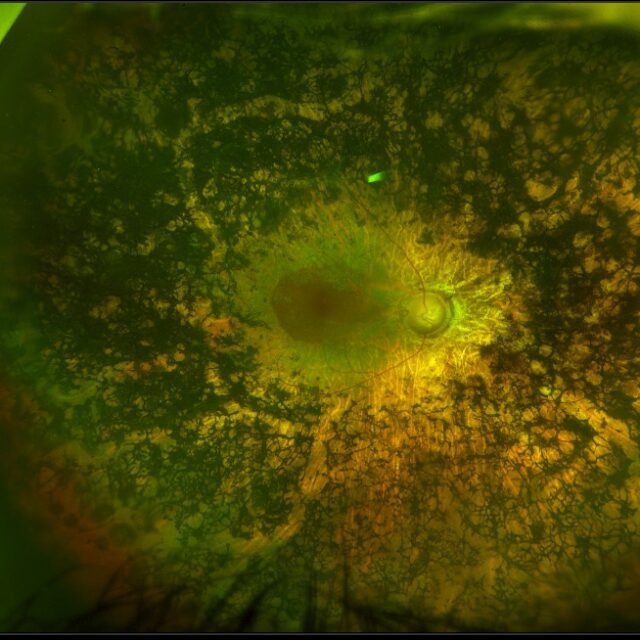
Спадкові дегенерації сітківки (СДС, англ. IRD — inherited retinal degenerations) — це група генетичних захворювань, які зумовлюють прогресивну втрату зору внаслідок загибелі фоторецепторів — світлочутливих клітин сітківки. Причиною цього є мутації в генах, критично важливих для функціонування та виживання фоторецепторів.
Генна терапія вже давно розглядається як перспективна стратегія для відновлення або збереження зору. Проте більшість існуючих методів орієнтовані на ранні стадії захворювання, коли ще не настала значна загибель фоторецепторів. Це створює серйозну прогалину в терапевтичних можливостях для пацієнтів, яким діагноз встановлюється на пізніших етапах.
Прорив у Penn Vet: потужні промотори для дегенерованої сітківки
Дослідники з Відділу експериментальної терапії сітківки Школи ветеринарної медицини Університету Пенсильванії (Penn Vet) у співпраці з іншими установами повідомили про створення нового набору високоспецифічних промоторів для фоторецепторів. Результати опубліковані в журналі Molecular Therapy.
Команду очолювали:
- д-р Рагхаві Судхарсан, доцент експериментальної офтальмології Penn Vet
- проф. Вільям А. Белтран, керівник відділу, професор офтальмології імені Корінн Р. Генрі Бауер
Вчені розробили чотири нові короткі ДНК-послідовності (промотори), які ефективно активують терапевтичні гени в паличках і колбочках навіть тоді, коли понад половина фоторецепторів уже втрачена.
«Ці промотори працюють як молекулярні перемикачі, які активують цільові гени безпосередньо в клітинах, що збереглися, забезпечуючи високу експресію навіть на пізніх стадіях захворювання», — пояснює Судхарсан.
Вищі за ефективністю, менші за розміром
У порівнянні зі стандартним промотором GRK1, нові конструкції продемонстрували вищу силу та специфічність експресії, зокрема промотори на основі гену GNGT2. Вони були активними як у паличках, так і в колбочках, і мають розмір менше 850 пар основ, що робить їх ідеальними для доставки за допомогою аденоасоційованого вірусу (AAV).
Більшість традиційних промоторів для колбочок є значно більшими і можуть не поміститися в межах обмеженого обсягу AAV-векторів.
«Малий розмір і клітинна специфічність знижують ризик побічних ефектів і зменшують потенційні імунні реакції — ключові фактори при розробці безпечної довготривалої терапії», — зазначив Белтран.
Як це вдалося?
Команда використала поєднання in silico моделювання, транскриптомного аналізу та in vivo тестування на великих тваринних моделях, які імітують людські форми IRD. Відповідно, тестування проводилося не в клітинних культурах чи органоїдах, а в повноцінних клінічно релевантних умовах.
Серед найбільш перспективних промоторів — ті, що отримані з генів GNGT2, IMPG2 та PDE6H, які демонстрували стабільну та високо специфічну експресію після доставки через AAV у сітківки собак з дегенеративними захворюваннями сітківки.
«Це дослідження відкриває новий шлях до генної терапії для пацієнтів на пізніх стадіях IRD — саме там, де наразі відчувається найбільший дефіцит ефективних методів лікування», — підсумовує Судхарсан.
Оригінальне дослідження було опубліковане в журналі Molecular Therapy 21 травня 2025 року.