Дослідники виявили методику безпосереднього перепрограмування клітин шкіри у світлочутливі фоторецептори (палички). Ці створені в лабораторії палички дозволили сліпим мишам виявляти світло після того, як клітини були введені в їх очі. Це дослідження, під спонсорством, National Eye Institute (NEI) було опубліковане 15 квітня 2020 року в журналі Nature. NEI є частиною National Institutes of Health.
До цих пір дослідники замінювали вмираючи фоторецептори в тваринних моделях, використовуючи клітини, які були отримані шляхом перетворення клітин шкіри або крові на стовбурові клітини, які вже в свою чергу перетворювались на фоторецептори. В новому дослідженні вчені показують, що існує можливість пропускати проміжний етап стовбурових клітин і безпосередньо перетворювати клітини шкіри в фоторецептори для пересадки в сітківку.
“Це перше дослідження, яке показало, що пряме хімічне перепрограмування може створити клітини типу тих, що є в сітківці, і це дає нам новішу та швидшу стратегію для розробки терапії вікової макулодистрофії та інших патологій сітківки, які викликані втратою фоторецепторів”, – сказав Anand Swaroop, Ph.D, старший дослідник та начальник NEI Neurobiology, Neurodegeneration, and Repair Laboratory, яка характеризувала перепрограмовані клітини фоторецепторів методом аналізу експресії генів.
“Користь, яку ми отримаємо негайно буде можливість швидко розробляти моделі хвороб для вивчення їх механізму. Нова стратегія також допоможе нам розробити кращі підходи до заміни клітин”, – продовжив він.
Протягом останнього десятиліття дослідники вивчали індуковані плюрипотентні стовбурові клітини (iPS). IPSC синтезуються в лабораторії із зрілих клітин, які відрізняються від тканин плода. І вони можуть використовуватись для виготовлення майже будь-якого типу клітин або тканин, які потребують заміни. Але протоколи перепрограмування клітин iPS можуть зайняти близько 6 місяців, перш ніж вони будуть готові до трансплантації. Для порівняння, пряме перепрограмування, описане у цьому дослідженні, перетворювало клітини шкіри у функціональні фоторецептори, готові до трансплантації, всього за 10 днів. Дослідники продемонстрували цю техніку на очах мишей, використовуючи клітини шкіри як самих мишей, так і людини.
Пряме перепрограмування передбачає “купання” клітин шкіри в коктейлі із п’яти малих молекулярних сполук, які разом хімічно опосередковують молекулярні шляхи, важливі для долі фоторецепторних клітин. Результатом цього є палички, які за зовнішнім видом та функціями імітують натуральні клітини.
Дослідники провели кількісний аналіз експресії генів, який показав, що гени, експресовані новими клітинами, були індентичними тим, що експресуються дійсними паличками. В той же час, гени, які стосуються функції шкіри, подавлялися. Дослідники пересадили ці клітини мишам із дегенерацією сітківки, а потім перевірили їх зіничний рефлекс, який є показником функції рецепторів після трансплантації. За умов слабкого освітлення звуження зіниці залежить від функції паличок. Протягом місяця після трансплантації 6 із 14 (43%) тварин продемонстрували гарне звуження зіниць при слабкому освітленні, в порівнянні із групою, якій не було проведено трансплантацію.
Крім того, проліковані миші, в яких звужувалась зіниця, були більш схильними до пошуків та проводження часу в темних просторах, аніж миші, в яких зіничний рефлекс не спостерігався, або ті, яким не проводилось лікування. Надавати перевагу темним просторам – поведінка, яка вимагає зору і відображає природну схильність мишей шукати безпечні темні місця.
“Навіть миші із сильно розвиненою дегенерацією сітківки, в яких живі фоторецептори залишились із малою імовірністю, продемонстрували відповідь на трансплантацію. Такі висновки свідчать про те, що отримане поліпшення було спричинене лабораторними рецепторами, а не допоміжним ефектом, який підтримував здоров’я існуючих фоторецепторів”, – сказав перший автор дослідження Biraj Mahato, Ph.D., науковий співробітник UNTHSC.
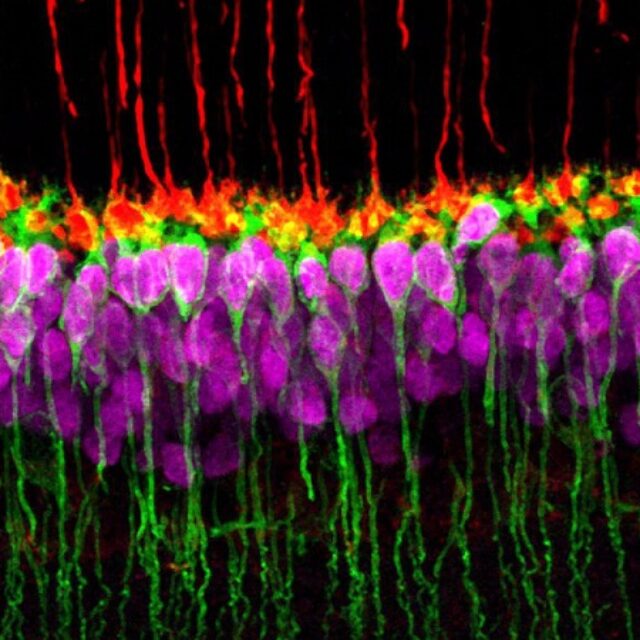
Через три місяці після трансплантації імунофлуоресцентні дослідження підтвердили виживання лабораторних фоторецепторів, а також їх синаптичні зв’язки із нейронами внутрішньої сітківки.

Зеленим відмічені пересаджені фоторецептори, які добре функціонували та інтегрувались у сітківку через три місяці після трансплантації
Подальші дослідження все ще залишаються необхідними для оптимізації протоколу, щоб збільшити кількість функціональних пересаджених рецепторів.
“Дуже важливо, що дослідники вирахували як опосередковується це пряме перепрограмування на клітинному рівні. Це розуміння допоможе дослідникам застосувати методику не тільки для клітин сітківки, а до багатьох інших типів клітин”, – сказав Anand Swaroop.
“Якщо ефективність цього прямого перетворення може бути підвищена, це може значно скоротити час для розробки потенційного продукту клітинної терапії або моделі захворювання”, – сказав Kapil Bharti, Ph.D., старший дослідник та голова Ocular and Stem Cell Translational Research Section в NEI.
Chavala із колегами планують проведення клінічного дослідження для перевірки клітинної терапії у людей із дегенеративними захворюваннями сітківки, такими як пігментний ретиніт.
Оригінальна стаття була опублікована на сайті National Eye Institute 15 квітня 2020 року.