Дослідники з Китаю успішно відновили зір мишей з пігментним ретинітом – однією з основних причин сліпоти у людей. У дослідженні, яке буде опубліковано 17 березня в Journal of Experimental Medicine, використовується нова, надзвичайно універсальна форма редагування геному на основі CRISPR з потенціалом для виправлення широкого спектру морбідогенних генетичних мутацій.
Дослідники раніше використовували редагування геному для відновлення зору мишей із генетичними захворюваннями, такими як вроджений амавроз Лебера, які вражають пігментний епітелій сітківки – шар ненейрональних клітин в оці, який підтримує фоторецепторні клітини світлочутливої палички та колбочки. Однак більшість успадкованих форм сліпоти, включаючи пігментний ретиніт, спричинені генетичними дефектами самих фоторецепторів.
«Можливість редагувати геном нервових клітин сітківки, особливо хворих або вмираючих фоторецепторів, надасть набагато переконливіші докази потенційного застосування цих інструментів редагування геному в лікуванні таких захворювань, як пігментний ретиніт», — говорить Кай Яо, професор Уханьського університету науки і технологій.
Пігментний ретиніт може бути спричинений мутаціями в понад 100 різних генах і, за оцінками, погіршує зір у 1 з 4000 людей. Хвороба починається з дисфункції та загибелі паличкоподібних клітин, що сприймають неяскраве світло, а потім поширюється на колбочкові клітини, необхідні для кольорового зору, що зрештою призводить до серйозної, необоротної втрати зору.
Яо та його колеги намагалися врятувати зір мишей з пігментним ретинітом, викликаним мутацією в гені, що кодує критично важливий фермент під назвою PDE6β. Для цього команда Яо розробила нову, більш універсальну систему CRISPR під назвою PESpRY, яку можна запрограмувати на коригування багатьох різних типів генетичних мутацій, незалежно від того, де вони відбуваються в геномі.
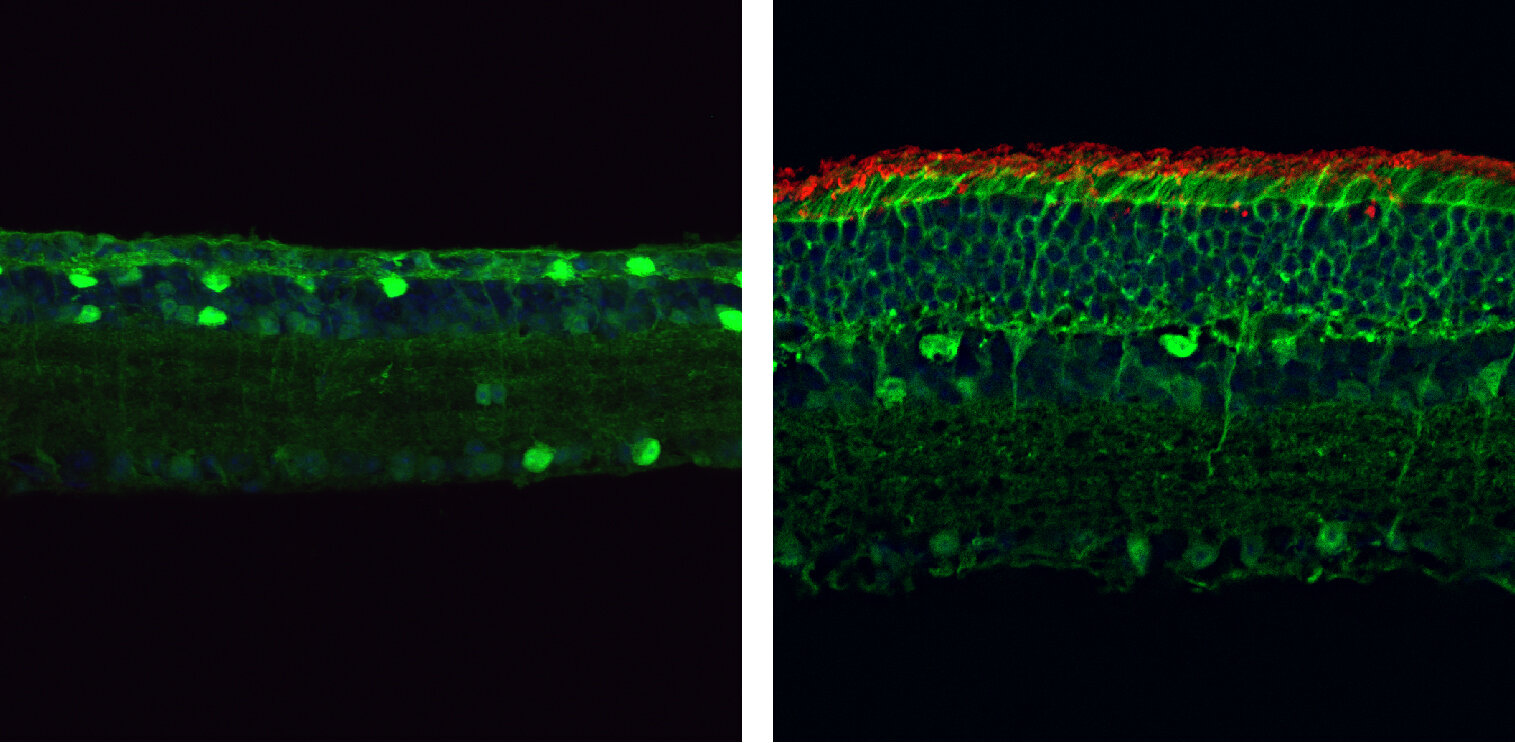
Після програмування націлювання на мутантний ген PDE6β система PESpRY змогла ефективно виправити мутацію та відновити активність ферменту в сітківці ока мишей. Це запобігло загибелі фоторецепторів паличок і колбочок і відновило їхні нормальні електричні реакції на світло.
Яо та його колеги провели різноманітні поведінкові тести, щоб підтвердити, що миші з редагованими генами зберігали свій зір навіть до похилого віку. Наприклад, тварини змогли знайти вихід із візуально керованого водяного лабіринту майже так само добре, як і звичайні, здорові миші, і показали типові рухи голови у відповідь на візуальні стимули.
Яо попереджає, що треба буде зробити ще багато роботи в майбутньому, щоб встановити як безпечність, так і ефективність системи PESpRY для людей. «Однак наше дослідження надає вагомі докази застосовності цієї нової стратегії редагування геному in vivo та її потенціал у різноманітних дослідженнях і терапевтичних контекстах, зокрема для спадкових захворювань сітківки, таких як пігментний ретиніт», — говорить Яо.
Оригінальна стаття була опублікована на порталі Medical Xpress 17 березня 2023 року.